Novos medicamentos podem “imitar” estrutura nanométrica do SARS-CoV-2
 Os vírus são nanopartículas naturais que interagem de modo preciso e eficiente com o maquinário biológico dos organismos e graças à características de estrutura muito bem distribuídas conseguem excelentes resultados de replicação. Pesquisadores do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), propõem olhar com maior atenção para a arquitetura das proteínas do SARS-CoV-2 observando em nanoescala para que sejam melhor compreendidas e aproveitadas no desenho de novas estratégias de produção de medicamentos. Nas últimas décadas, a ciência avançou a um ponto de controle surpreendente sobre materiais em nanoescala desenvolveu plataformas sofisticadas capazes de contribuir significativamente para melhorar resultados terapêuticos. Um dos maiores desafios é desenhar estratégias de direcionamento de nanopartículas que minimizem as eventuais vulnerabilidades de interação delas fora dos alvos específicos. O artigo, recém publicado na revista científica Nano Today , descreve as características estruturais do SARS-Cov-2 que poderiam ser copiadas no desenho de uma possível nanopartícula sintética, racionalmente otimizada para obter a melhor capacidade de direcionamento.
Os vírus são nanopartículas naturais que interagem de modo preciso e eficiente com o maquinário biológico dos organismos e graças à características de estrutura muito bem distribuídas conseguem excelentes resultados de replicação. Pesquisadores do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), propõem olhar com maior atenção para a arquitetura das proteínas do SARS-CoV-2 observando em nanoescala para que sejam melhor compreendidas e aproveitadas no desenho de novas estratégias de produção de medicamentos. Nas últimas décadas, a ciência avançou a um ponto de controle surpreendente sobre materiais em nanoescala desenvolveu plataformas sofisticadas capazes de contribuir significativamente para melhorar resultados terapêuticos. Um dos maiores desafios é desenhar estratégias de direcionamento de nanopartículas que minimizem as eventuais vulnerabilidades de interação delas fora dos alvos específicos. O artigo, recém publicado na revista científica Nano Today , descreve as características estruturais do SARS-Cov-2 que poderiam ser copiadas no desenho de uma possível nanopartícula sintética, racionalmente otimizada para obter a melhor capacidade de direcionamento.
Simetria e homogeneidade
O SARS-CoV-2 usa uma glicoproteína S, chamada de spyke, para mediar a entrada nas células hospedeiras. Essa proteína está distribuída de acordo com padrões de geometria e simetria bem específicos, na superfície do vírus. Em nanopartículas produzidas em laboratório essa distribuição de ligantes costuma ser mais aleatória e portanto, algumas vezes, muito mais densa. Nos vírus, esse meticuloso arranjo, com os espaços ordenados (15 nm) entre as proteínas, otimiza a replicação e transforma uma série de interações fracas em fortes, o que aumenta as chances de entrada nas células. De acordo com o artigo, o espaço parece fundamental para o aumento de probabilidade de interação, já que permite que as estruturas flexíveis das proteínas S e ACE2 assumam diferentes orientações espaciais favorecendo os pontos de contato ativos. Essa flexibilidade de movimentos não é normalmente encontrada em outros coronavírus.
Eficiência no direcionamento
A principal porta de entrada para as infecções por SARS-CoV-2 costuma ser o nariz, de onde o vírus se espalha para todo o trato respiratório. Nesse ponto se encontram alojadas nas células epiteliais dos cílios móveis a proteína ACE2, um dos mais conhecidos receptores do novo coronavírus. O comprimento dos cílios é cerca de 50 vezes o tamanho do vírus (~ 5 μm vs. ~ 100 nm) contendo receptores para fixação de vírus. O SARS-CoV-2 apresenta uma afinidade de ligação 10 vezes mais forte para ACE2 do que SARS-CoV embora ambos compartilhem 76% da sequência genética da proteína S.
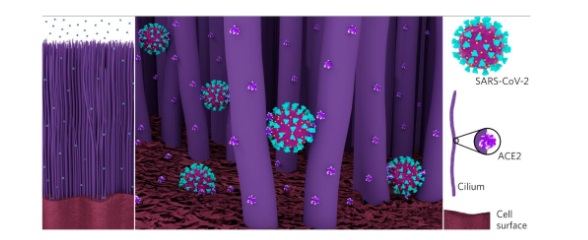
Inspiração da natureza para nanomedicina
De acordo com os pesquisadores, um dos maiores desafios para imitar a natureza na produção de nanopartículas sintéticas está no controle preciso do organização de superfícies dessas estruturas. Para se obter algo similar ao nível organizacional viral, os designers de nanomateriais precisam superar os atuais métodos e incorporar abordagens sintéticas ainda mais precisas, como estratégias de funcionalização que permitam o controle do distanciamento médio entre grupos bioativos. Outro desafio importante está relacionado com a alta seletividade, que garante a precisa “responsividade” aos eventos biológicos. Os receptores precisam superar obstáculos de interação e passar ilesos pelo reconhecimento do sistema imunológico até que encontrem os alvos que permitam a entrada nas células. O artigo conclui que novas soluções de combate ao SARS-Cov-2 deveriam considerar a combinação racional de conhecimentos relacionados aos arranjos estruturais da superfície do vírus para que, em contato com o receptor, promovam reações pontuais com maior eficiência.