Mutação ligada à epilepsia grave revela impactos inéditos no desenvolvimento do cérebro
Uma alteração minúscula no DNA pode ter efeitos profundos no cérebro em formação. Foi justamente isso que pesquisadoras da Fiocruz investigaram ao estudar uma mutação genética associada a formas graves de epilepsia infantil. Os resultados foram publicados na revista Scientific Reports, do grupo Nature.
O estudo se debruça sobre a variante R87C do gene CYFIP2, já relacionada à encefalopatia epiléptica, um conjunto de distúrbios neurológicos raros caracterizados por crises frequentes e prejuízos no desenvolvimento cognitivo. O que ainda não se sabia com clareza era como essa mutação interfere, na prática, no desenvolvimento das células do cérebro humano.
Para responder a essa pergunta, a equipe utilizou uma das ferramentas mais avançadas da biologia molecular, a edição genética por CRISPR. A partir de células-tronco pluripotentes humanas, capazes de se transformar em diferentes tipos celulares, os pesquisadores criaram modelos que simulam etapas do desenvolvimento cerebral. Essas células foram diferenciadas em células progenitoras neurais, neurônios corticais e estruturas tridimensionais conhecidas como organoides cerebrais, que reproduzem aspectos do cérebro em formação.
Os resultados mostram que os efeitos da mutação aparecem cedo. As células progenitoras neurais com a variante apresentaram menor capacidade de se movimentar e alterações em sua forma, indicando problemas na organização interna responsável pelo movimento celular. Esse processo é fundamental para que as células ocupem corretamente seus lugares durante a formação do cérebro.
Curiosamente, quando analisados em culturas bidimensionais tradicionais, os neurônios derivados dessas células não apresentaram diferenças significativas em relação aos neurônios sem a mutação, tanto em sua aparência quanto em sua atividade elétrica. Mas o cenário muda quando o modelo se aproxima mais da realidade biológica.
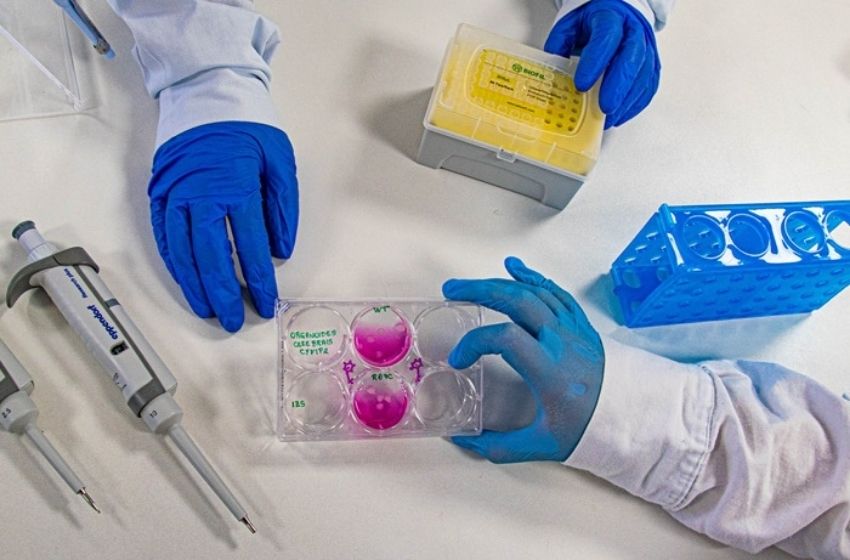
Nos organoides cerebrais, que oferecem uma representação mais complexa do desenvolvimento, as pesquisadoras observaram alterações importantes. Houve redução nos níveis da proteína CYFIP2, crescimento anormal dessas estruturas e uma diminuição precoce das células progenitoras. Na prática, isso sugere que o “estoque” de células responsáveis por gerar novos neurônios pode se esgotar antes do tempo, comprometendo a formação adequada do cérebro.
“O uso de modelos tridimensionais foi essencial para revelar alterações que não eram visíveis em sistemas mais simples”, explica a pesquisadora Patrícia Shigunov, coordenadora do estudo na Fiocruz Paraná. Segundo ela, essa diferença reforça a importância de utilizar abordagens mais sofisticadas para investigar doenças neurológicas. O artigo é assinado por Isabelle Zaboroski da Silva e Evelin Brandão da Silva, estudantes do Programa de Pós-Graduação em Biociências e Biotecnologia da Fiocruz Paraná, além de colaboradores da Case Western Reserve University, nos Estados Unidos, e da Pontifícia Universidade Católica do Paraná (PUCPR).
O trabalho dá continuidade a uma linha de pesquisa sobre doenças raras já desenvolvida pelo grupo, que anteriormente produziu células-tronco a partir de amostras de pacientes. Ao longo do projeto, um dos principais desafios foi justamente identificar diferenças claras entre células com e sem a mutação, especialmente em modelos bidimensionais.
Para superar essa limitação, os cientistas desenvolveram uma linhagem celular isogênica por edição genética, permitindo comparações mais precisas e reduzindo interferências de outras variações genéticas. A estratégia aumentou a robustez dos resultados e reforçou a associação direta entre a mutação e os efeitos observados. A pesquisa também fortaleceu a colaboração internacional, especialmente com a pesquisadora Helen Cristina Miranda (Case Western Reserve University), ampliando o acesso a novas técnicas e infraestrutura em neurogênese.
“Estamos muito entusiasmados por publicar os primeiros achados desta variante em um modelo neuronal humano, um passo vital para desvendarmos como ela realmente atua. Foi um projeto tecnicamente desafiador e uma jornada intensa, mas ver o progresso no conhecimento sobre doenças raras torna cada etapa extremamente recompensadora”, afirma Isabelle Zaboroski da Silva.
Para Evelin Brandão da Silva, o estudo marca apenas o início de um caminho mais longo. “Foi uma experiência árdua, que reforça a importância de investigar o que ainda não é totalmente compreendido e como isso pode gerar impactos duradouros no futuro, sendo apenas o início de novas descobertas.”
Mais do que aprofundar o entendimento sobre uma mutação específica, o estudo abre novas perguntas sobre o desenvolvimento cerebral e aponta caminhos para futuras pesquisas. Em um campo onde ainda há muitas lacunas, cada avanço ajuda a aproximar a ciência de estratégias mais eficazes para compreender e, no futuro, tratar doenças neurológicas raras. (Com informações da Agência Fiocruz)