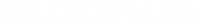
Biópsia líquida amplia possibilidades de terapias para pacientes com câncer
A técnica de diagnóstico oncológico denominada biópsia líquida (análise de DNA tumoral no sangue periférico) também é capaz de detectar alterações genéticas passíveis de tratamento alvo em pacientes com diferentes tipos de tumores sólidos avançados, e não apenas em câncer de pulmão, para o qual o uso já foi amplamente reconhecido. A conclusão vem de dois estudos desenvolvidos no laboratório Personal Diagnósticos Moleculares e de Precisão.
Os resultados estarão disponíveis online, em junho, na sessão pôster do congresso 2021 da American Association for Cancer Research – AACR, entidade considerada a mais importante do mundo no estudo da oncologia translacional.
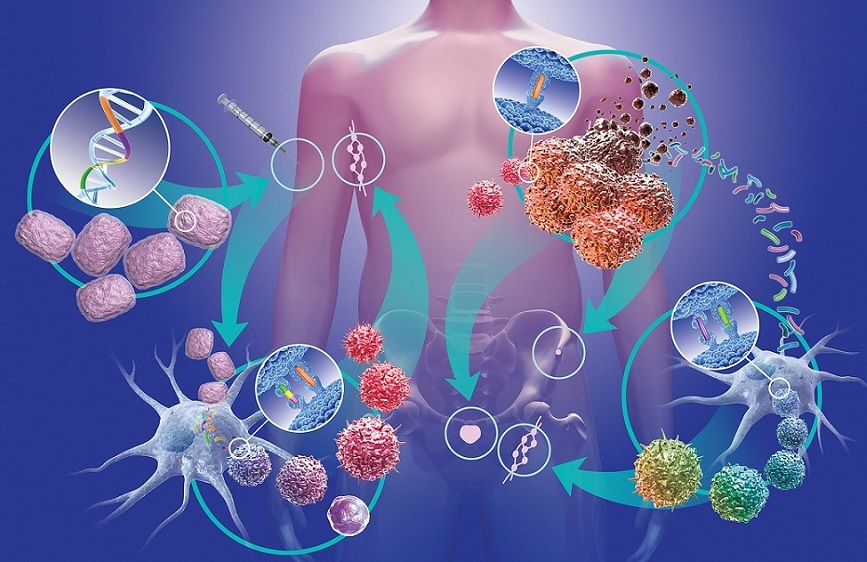
Os pesquisadores – o oncogeneticista e professor da Universidade Federal de Minas Gerais – UFMG André Márcio Murad, e os pesquisadores do Laboratório Personal a bióloga e PhD em Genética Juliana Carneiro e o oncogeneticista José Cláudio Casali da Rocha – avaliaram em dois estudos diferentes a capacidade das plataformas PCR Digital em Gotas (dd-PCR Digital) e Sequenciamento de Nova Geração – NGS com tecnologia de captura híbrida identificarem alvos-tumorais presentes no DNA tumoral circulante no sangue periférico dos participantes.
Essa análise é chamada de somática, o que significa que está sendo avaliado somente o DNA presente no tumor, ao contrário da análise germinativa, que avalia o DNA do paciente em busca de alterações herdadas.
Como resultados, os cientistas encontraram taxas de sucesso consideráveis em ambas as plataformas. “Ao realizarmos dois estudos diferentes sobre duas técnicas de biópsia líquida, conseguimos encontrar bons resultados em cada um deles,” comenta o pesquisador e oncologista André Márcio Murad.
Resultados do PCR Digital em Gotas
O estudo reuniu os resultados de análises de 10 genes feitas com tecnologia dd-PCR Digital com sangue de 108 pacientes com tumores de mama, intestino (colorretal), melanoma, estômago e de Estroma Gastrointestinal – GISTs. Com isso, os pesquisadores identificaram que em 35% dos pacientes havia variações genéticas para as quais existem tratamentos específicos – sejam comercialmente disponíveis, por acesso expandido ou por meio de estudos clínicos em desenvolvimento no Brasil.
Resultados do painel em NGS – Guardant360
Por sua vez, na análise em NGS, com o painel Guardant360, que é capaz de ler até 74 genes, foi encontrada uma taxa de sucesso de 64%, a partir das análises de sangue de 45 pacientes. “Um número menor de participantes e um universo maior de alterações genéticas identificáveis resultaram na maior taxa de sucesso. Esse estudo de NGS é uma das maiores experiências nacionais com esse tipo de tecnologia e abre caminho para sua ampla utilização”, avalia.
Análises
Para Murad, os dados encontrados são importantíssimos por serem genuinamente nacionais e refletirem mais adequadamente o perfil genético encontrado entre os brasileiros. “Muitas vezes, as tecnologias existem e são utilizadas nos EUA e Europa sem que haja uma validação com pacientes brasileiros. As características dos tumores que ocorrem no Brasil não são necessariamente idênticas às que se observam entre pacientes norte-americanos e europeus. Temos nossa própria casuística, nossa própria genômica. Por isso, precisamos ter dados que reflitam de fato esse perfil e permitam indicar ferramentas mais assertivas.”, defende.
De forma prática, os dados gerados pelos pesquisadores permitem aos oncologistas solicitarem as biópsias líquidas com maior segurança, o que repercute em maiores chances de sobrevida e qualidade de vida para pacientes com tumores avançados. Com essas informações, os oncologistas conseguem elaborar estratégias mais personalizadas e individualizadas, definindo terapias-alvo, medicamentos ou associação de medicamentos conforme o perfil genético identificado. Além disso, a exposição à toxicidade também pode ser minimizada.
“Mostramos que são exames factíveis, viáveis, acessíveis e confiáveis. É muito satisfatório conseguir identificar, por meio da biópsia líquida, um biomarcador que sugere um novo tratamento em um paciente com doença totalmente refratária, que foi submetido a vários tipos de tratamentos sem resultados satisfatórios. E agora mostramos que, tanto a biópsia líquida com NGS em um painel mais robusto como Guardant360, quanto a dd-PCR, que é mais pontual, podem ser utilizadas para esse fim. Isso é esperança de vida”, observa Murad.
O que é biópsia líquida
A biópsia líquida é uma tecnologia minimamente invasiva para a detecção de biomarcadores moleculares sem a necessidade de procedimentos mais invasivos como biópsias e cirurgias. Ela permite aos médicos descobrirem uma série de informações sobre uma doença ou um tumor através de uma extração de uma simples amostra de sangue. Conforme detalha Murad, as células tumorais circulantes ou traços do RNA ou do DNA podem fornecer informações valiosas sobre quais tratamentos são mais prováveis e efetivos para o paciente.
“Por isso novas tecnologias que elevam a sensibilidade da biópsia líquida têm sido utilizadas, como o emprego do PCR digital (como as técnicas de dd-PCR – digital em gotas e o BEAMING – beads, emulsions, amplification and magnetics), e o NGS (sequenciamento de nova geração) com tecnologia de captura híbrida e sequenciamento digital.”, acrescenta o oncogeneticista.
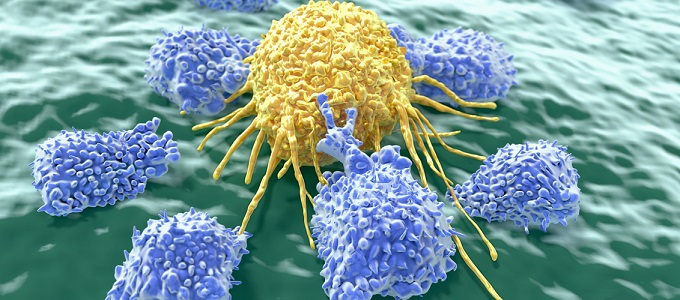
Como funciona a Biópsia Líquida
Quando um médico suspeita do diagnóstico de câncer em um paciente, ele solicita uma biópsia daquela região, que basicamente é a retirada de parte do tecido para análise em laboratório com o objetivo de identificar se existem células cancerosas naquele local. Esse material também pode ser usado para identificar quais tipos de mutações estão ocorrendo no tumor.
Mas, quando os tratamentos não fazem o efeito esperado e o tumor evolui, entra em campo a biópsia líquida, um exame feito a partir da coleta de 20 a 30 ml de sangue. Com esse material biológico é possível extrair até 10 nanogramas de DNA e RNA tumorais circulantes no sangue periférico, para avaliar a presença de variações que servem de biomarcadores. É possível coletar esse DNA tumoral fora do local de origem do tumor devido a apoptose das células tumorais: conforme morrem, seu material genético é liberado na corrente sanguínea do paciente.
Além de evitar que o paciente se submeta a uma nova cirurgia para retirada de mais tecido, o que apresenta riscos como agravamento de lesões por excesso de manipulação, contaminação do tecido saudável ao redor do tumor, hemorragias, infecções e formação de fístulas, a biópsia líquida tem o diferencial de apresentar o “retrato” mais atual daquele tumor.
“Cada tumor passa por consecutivas mutações e em meses pode estar bem diferente do que era no começo. Por ser feito com material novo (DNA Circulante), essa tecnologia consegue fornecer um retrato atual do tumor, ao contrário da biópsia tecidual feita com parafina arquivada, que fornece informações antigas”, explica o oncogeneticista.
Além disso, complementa o pesquisador, “às vezes o pedaço de tecido retirado na biópsia tradicional nem sempre é o material genético ideal para achar uma terapêutica, pois alterações podem estar presentes em outra região do tumor ou em outras regiões metastáticas. Já na biópsia líquida temos acesso a uma amostra mais geral, possibilitando identificar variantes vindas de diferentes pontos de metástase, e que podem levar a escolha de um tratamento específico.”
Diferenças entre as plataformas NGS e dd-PCR Digital
Antes de entender a diferença entre o NGS com captura híbrida e o PCR Digital em Gotas é necessário saber que ambas as técnicas podem ser feitas com parafina (tecido do tumor) ou sangue, tendo nesse caso os benefícios citados acima. Além disso, os dois utilizam a Reação da Polimerase em Cadeia (Polymerase Chain Reaction em inglês), que, resumindo bem, é uma técnica da biologia molecular para copiar fitas de DNA. Nos estudos feitos pelo laboratório foram utilizadas somente as técnicas de biópsia líquida, ou seja, com amostras de DNA e RNA tumoral coletadas do sangue dos pacientes para análises de mutações presentes no DNA do tumor (somáticas).
Sequenciamento de Próxima ou Nova Geração – NGS
O Sequenciamento de Próxima ou Nova Geração – NGS (Next-Generation Sequencing) também é chamado de Sequenciamento Massivo em Paralelo ou Sequenciamento de Alta Performance. Esse tipo de tecnologia se caracteriza pela capacidade de ler bilhões de fragmentos de DNA ao mesmo tempo.
Com o NGS pode-se sequenciar o genoma inteiro de uma ou várias pessoas ou apenas áreas específicas de interesse, incluindo todos os aproximadamente 20 mil genes codificadores ou um pequeno número de genes individuais. Em qualquer uma dessas opções, o NGS consegue detectar alterações como substituições, inserções e deleções de nucleotídeos na sequência do DNA.
PCR Digital em Gotas
Por sua vez, o PCR Digital em Gotas é um método muito mais sensível que permite procurar uma variação específica ou algumas poucas variações que são de interesse no caso de um determinado paciente. Esse painel digital oferece uma maior sensibilidade para a detecção de alterações gênicas em amostras com quantidades restritas de DNA.
No sistema de dd-PCR Digital, cada amostra é dividida em 20 mil gotas e cada gota tem seu DNA ou RNA amplificado, sendo que as alterações genéticas procuradas são facilmente detectadas por fluorescência. Quando o equipamento lê cada uma dessas gotas, uma por uma, consegue especificar quantas delas continham DNA com mutação e quantas tinham DNA normal, o que é importante para os médicos, por exemplo, saberem se o tumor está regredindo.
“Entre outras indicações, o PCR Digital pode ser utilizado, por exemplo, quando o médico quer saber se tem mutação especificamente no gene HER2 ou se há uma mutação de resistência específica no paciente que não responde mais ao tratamento. Então, são análises direcionadas. Esse teste é capaz de dar uma quantificação absoluta, dizer o percentual de DNA tumoral e a carga tumoral circulante no sangue periférico que o paciente tem. É possível com essa tecnologia definir genes e marcadores específicos para monitorar o paciente que já teve as mutações identificadas anteriormente, o que é útil para avaliar a resposta ao tratamento”, explica a bióloga Juliana Carneiro.
Segundo os especialistas, a plataforma dd-PCR Digital oferece uma sensibilidade muito maior, o que significa que possui maior capacidade de identificar as alterações genéticas, quando comparada ao PCR convencional e mesmo a algumas metodologias que empregam o NGS. Além da alta sensibilidade e do baixo custo, a técnica se diferencia das demais pela rapidez de execução (leitura em cerca de 48 horas).
“Na plataforma NGS, além do maior custo e tempo de leitura, que depende de bioinformática, os resultados são obtidos em torno de 10 a 14 dias, mas também é bastante interessante.”, finaliza.
Onde acessar os estudos
Os pôsteres sobre cada um dos estudos estarão disponíveis online entre 10 de abril e 21 de junho, na plataforma www.aacr.org em programação/biomarcadores/biópsia. Também estarão disponíveis slides explicativos e áudios sobre cada um dos estudos.